

3月27日,巴瑞替尼片(baricitinib)正式获得国家药品监督管理局(NMPA)批准,用于成人重度斑秃的系统性治疗,是国内首个且唯一用于系统性治疗重度斑秃的创新靶向药物,可帮助患者获得显著的毛发再生,对头发、眉毛、睫毛等区域具有持续性的改善作用。
早在2022年6月14日,美国FDA宣布,批准礼来公司(Eli Lilly)和Incyte公司联合开发的口服JAK抑制剂巴瑞替尼(baricitinib)上市,用于治疗严重斑秃成人患者。这是FDA批准用于治疗斑秃的首款系统性疗法。
巴瑞替尼是一款口服JAK抑制剂,它已经在超过75个国家和地区获批用于治疗类风湿性关节炎,并且在超过50个国家和地区获批用于治疗中重度特应性皮炎。
2020年,针对斑秃的适应症,巴瑞替尼获得FDA授予的突破性疗法认定和优先审评资格。2021年3月,它在治疗斑秃的3期临床试验BRAVE-AA2中获得积极结果,成为首个在治疗斑秃的3期临床试验中被证明可促进头发再生的口服JAK抑制剂。
2021年4月,礼来公司和Incyte公司宣布,其巴瑞替尼在治疗重度斑秃患者的第二项3期临床试验BRAVE-AA1中获得积极结果。基于这些结果,礼来公司在当年下半年向美国FDA提交补充新药申请(sNDA),使用巴瑞替尼用于临床治疗斑秃。
斑秃(alopecia areata,AA)是全球发病率第二高的脱发症状,全球大约有1.47亿患者,中国患者约有400万。它是一种自身免疫性疾病,由于免疫系统攻击毛囊,导致头皮、脸部或身体其他部分的毛发部分或完全脱落。斑秃症状经常在儿童时期就会发作,任何年龄、性别和种族的人群都可能患上斑秃。
巴瑞替尼的疗效和安全性在两项随机双盲,含安慰剂对照的临床试验中得到评估。参加这些试验的患者基线时至少50%的头发脱落超过6个月。
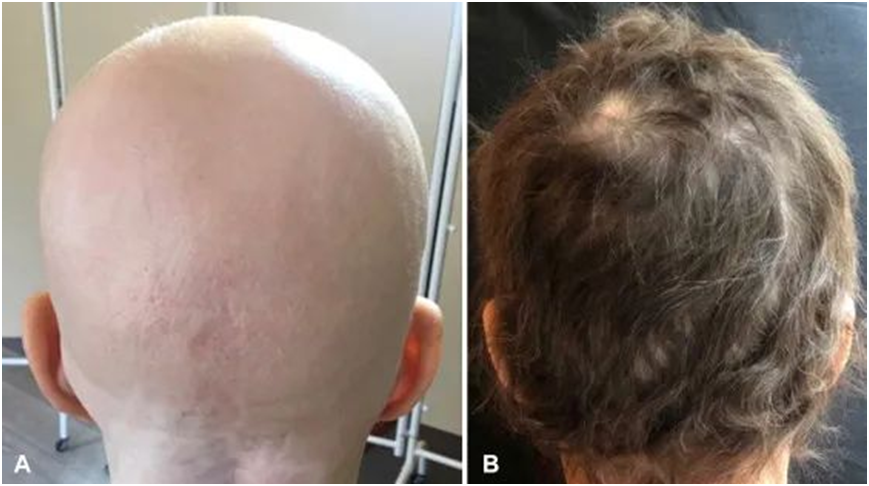
治疗前与治疗8个月后(来自案例报告)
试验结果显示,接受治疗36周后,在两项临床试验中,大约三分之一接受剂量为4 mg的巴瑞替尼治疗的患者达到头皮毛发覆盖面积超过80%(BRAVE-AA1=35.2%,BRAVE-AA2=32.5%),而安慰剂组的数值分别为5.3%(BRAVE-AA1)和2.6%(BRAVE-AA2)。同时,约三分之一的患者达到眉毛或睫毛完全再生或者没有明显缺失的指标。

东盟制药
2017年10月,老挝东盟制药(TLPH)生产的巴瑞替尼获老挝卫生部食品药品司(FDD)批准上市,用于治疗类风湿性关节炎和斑秃,均获得显著的效果。
作为老挝境内最早和规模最大的仿制药公司,东盟制药坚持“选好药、造好药”的价值理念,持续为“一带一路”沿线国家提供“安全、高效、经济可负担”的药物解决方案。