

2021年10月21日,老挝卫生部食品药品司(FDD)正式批准由老挝东盟制药(TLPH)生产的尼拉帕利(Niraparib)片剂上市销售,商品名为Nizela。这是东盟制药2021年第5款获批上市的一线抗癌药物。
尼拉帕利(Nizela)
 尼拉帕利的药品批准文号
尼拉帕利的药品批准文号
尼拉帕利是葛兰素史克(GSK)收购TESARO公司获得的PARP抑制剂。PARP抑制剂是通过抑制PARP介导的DNA损伤修复反应(DDR),杀伤癌细胞的靶向疗法。利用“合成致死”原理,它们能够在杀伤癌细胞的同时,不对健康细胞产生影响。
尼拉帕利最早于2017年3月获FDA批准,用于对铂类化疗产生完全或部分缓解的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌的维持治疗,是首个获批用于所有铂敏感复发性卵巢癌患者维持治疗的PARP抑制剂。
根据TESARO公司此前发布的III期临床数据显示,尼拉帕利对有BRCA基因突变的卵巢癌,每日口服尼拉帕利一次,中位无进展生存期为21个月,而对照组(使用化疗)的病人,只有5.5个月,前者是后者的接近的4倍,而对于未突变患者,也有9.3个月,超过安慰剂的两倍。
2019年10月24日,FDA批准尼拉帕利(Niraparib)扩大适应症,用于治疗接受过3种或以上化疗的同源重组缺陷(HRD)阳性的晚期卵巢癌患者、输卵管癌或原发性腹膜癌患者。
此次尼拉帕利扩大适应证是基于多中心、单臂、II期QUADRA研究,该研究旨在评估尼拉帕利用于四线及以上卵巢癌的疗效。
研究结果表明——
- 尼拉帕利在四线及以上卵巢癌人群中显示出明显疗效。主要研究人群中(HRD阳性、铂敏感、4或5线,n=47),总缓解率为28%,中位缓解持续时间为9.2个月。
- 在铂敏感患者中,BRCA突变患者ORR为39%,HRD阳性患者ORR为26%;在铂耐药或难治患者中,BRCA突变患者ORR为27%,HRD阳性患者ORR为10%。
2020年2月25日, GSK公司宣布,美国FDA已经接受该公司为PARP抑制剂尼拉帕利递交的补充新药申请(sNDA)。这一申请寻求使用尼拉帕利作为维持疗法,一线治疗对铂基化疗产生响应的晚期卵巢癌患者。FDA将使用实时肿瘤学审评(RTOR)试点项目对这一申请进行评估,有望尽早完成对这一申请的审评。
卵巢癌被称为“沉默的杀手”,是严重影响妇女生命健康的三大恶性肿瘤之一,因卵巢位于盆腔深处,难以扪及或筛查,多数患者确诊时已是晚期,其病死率位列三大妇科恶性肿瘤之首。
东盟制药高度关注女性癌症治疗领域。2017年,东盟制药奥利帕尼(Olaparib)胶囊剂上市,获得良好的市场反应;2021年9月,奥拉帕尼片剂上市;10月,尼拉帕利获批。至此,东盟制药同时拥有奥利帕尼(胶囊剂+片剂)、尼拉帕利两种用于一线治疗的PARP抑制剂。
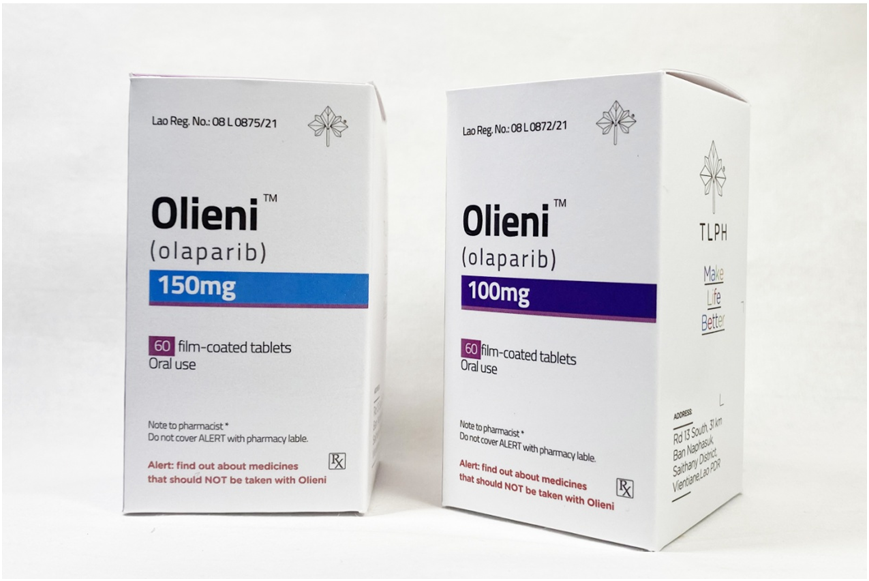
奥拉帕尼(片剂)

 东盟制药(TLPH)GMP证书
东盟制药(TLPH)GMP证书
东盟制药(TLPH)是老挝境内最早和规模最大的仿制药生产企业,目前已经获批的药品超过50款,大部分为全球领先的一线药物。近两年来,东盟制药克服疫情影响,不断加大高品质药物研发与生产投入,持续为“一带一路”沿线国家提供“安全、高效、经济可负担”的药物解决方案。